جواب آزمایش کنید صفحه 15 علوم تجربی نهم
هدف: تهیهٔ بلور
وسایل و مواد لازم: بشر، نخ، گیرهٔ فلزی، سدیم کلرید، کات کبود، شکر، آب مقطر، عینک، دستکش
روش اجرا:
الف) سه بشر ۱۰۰ میلیلیتری بردارید و درون هر کدام ۲۰ میلیلیتر آب مقطر داغ بریزید.
ب) درون هر بشر به طور جداگانه یک قاشق چایخوری از کات کبود، سدیم کلرید و شکر بیفزایید و آن قدر هم بزنید تا محلولهای شفاف به دست آیند این عمل را تا آنجا که مواد جامد حل شوند، ادامه دهید.
پ) یک گیره بردارید و با استفاده از نخ و مداد، آن را درون محلول آویزان کنید.
ت) بشرها را کنار پنجره بگذارید و پس از چند روز بلورهای تشکیل شده را مشاهده کنید. نتیجهٔ مشاهدهٔ خود را بنویسید.
کم کم بلورهای کوچکی به وجود آمده و با گذشت زمان بزرگتر میشوند.
آیا بلورهای این سه ماده شبیه هم هستند؟ چه تفاوتهایی با هم دارند؟
خیر، در شکل بلور - رنگ بلور - اندازه بلور - شکنندگی بلورها فرق دارند چون نوع ماده، غلظت ماده، دمای محلول سبب تفاوتهای بالا میگردد.
جواب آزمایش کنید صفحه 15 علوم تجربی نهم
هدف: بررسی رسانایی الکتریکی آب مقطر و محلول آبی چند ماده
وسایل و مواد لازم: بشر، سیم، منبع تغذیه (باتری قلمی یا کتابی)، لامپ ۱/۵ ولتی، میلهٔ کربنی، قاشقک، آب مقطر، سدیم کلرید، کات کبود، شکر، اتانول، عینک، دستکش
روش اجرا:
الف) یک مدار الکتریکی درست کنید.
ب) درون یک بشر مقداری آب مقطر بریزید و میلههای کربن را داخل آن قرار دهید (توجه کنید میلهها با هم در تماس نباشند.) مشاهدههای خود را بنویسید.
هیچ اتفاقی نمیافتد چون آب مقطر رسانای جریان الکتریسیته نیست.
پ) اکنون با استفاده از قاشقک، به اندازهٔ نصف قاشق چایخوری درون آب مقطر نمک خوراکی بیفزایید. چه چیزی مشاهده میکنید.
لامپ روشن و جریان در مدار برقرار میشود چون محلول آب و نمک رسانای جریان الکتریسیته است.
ت) قسمت پ آزمایش را با افزودن شکر، اتانول و کات کبود به آب مقطر تکرار کنید. مشاهدههای خود را یادداشت و جدول زیر را پر کنید.
| نام ماده | آب مقطر | محلول نمک خوراکی | محلول شکر در آب | محلول اتانول | محلول کات کبود در آب |
|---|---|---|---|---|---|
| رسانایی الکتریکی | ندارد | دارد | ندارد | ندارد | دارد |
جواب آزمایش کنید صفحه 16 غلوم تجربی نهم
هدف: بررسی حرکت یونها در آب
وسایل و مواد لازم: ظرف شیشهای (پتری)، پنس، آب مقطر، سدیم هیدروکسید، کات کبود
روش اجرا:
الف) درون ظرف پتری تا نیمه آب مقطر بریزید.
ب) با استفاده از پنس یک دانه بلور سدیم هیدروکسید را بردارید و به آرامی در کنار دیوارهٔ ظرف پتری درون آب قرار دهید.
پ) با استفاده از پنس یک دانه بلور کات کبود بردارید و آن را درون ظرف پتری و کنارهٔ دیواره و درست روبه روی بلور سدیم هیدروکسید قرار دهید. مدتی صبر کنید و مشاهدات خود را بنویسید.
- تغییر رنگ نشانهٔ چیست؟
تشکیل مادهٔ زرد رنگ سرب یدید در وسط ظرف
- معادلهٔ نوشتاری تغییر شیمیایی انجام شده به صورت زیر است.
فراوردهها = کات کبود + سدیم هیدروکسید
فراوردهها = یون مس، یون سولفات + یون سدیم، یون هیدروکسید
بر اساس این معادله، اگر یونهای مس و هیدروکسید به یکدیگر برسند، با هم واکنش میدهند. حال توضیح دهید از تشکیل رنگ جدید درون ظرف چه نتیجهای میگیرید؟
چون یونهای سرب و یُد از سمت بلورها شروع به حرکت و پخش شدن در اطراف و به سمت وسط ظرف میکنند و وقتی به وسط ظرف میرسند با ترکیب با هم ترکیب یونی زرد رنگ سرب یدید را میسازند.
- با توجه به نتیجهٔ این آزمایش توضیح دهید، چرا محلول نمکها رسانای جریان الکتریکی است؟
زیرا یونهای حاصل از آنها در محلول حرکت میکنند و سبب برقراری جریان الکتریکی در محلول میشوند.
جواب فعالیت صفحه 18 علوم تجربی نهم
شکلهای زیر آرایش الکترونی هر یک از ذرهها را در واکنش فلز سدیم با گاز کلر، پیش و پس از تغییر شیمیایی نشان میدهند.
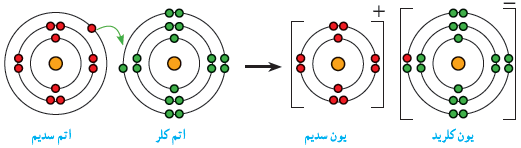
با بررسی شکلها: الف) جدول زیر را کامل کنید.
| نام ذره | اتم سدیم | یون سدیم | اتم کلر | یون کلر |
|---|---|---|---|---|
| مشخصات ذره | ||||
| تعداد الکترون | 11 | 10 | 17 | 18 |
| تعداد الکترون در مدار آخر | 1 | 8 | 7 | 8 |
| آیا مدار آخر ذره پر شده است؟ | خیر | بله | خیر | بله |
ب) کدام اتم الکترون از دست داده و کدام یک الکترون گرفته است؟
اتم سدیم الکترون از دست داده و اتم کلر یک الکترون گرفته است.
پ) هر یک از اتمهای سدیم و کلر چند الکترون مبادله کردهاند؟
یک الکترون بین خود مبادله میکنند.
ت) نماد شیمیایی یونهای سدیم وکلرید را بنویسید.
+Na (یون سدیم)، -CL (یون کلرید)
پ) ملاکی برای گرفتن یا دادن الکترون توسط اتم ها مشخص کنید.
اگر اتمی در مدار آخر خود الکترونهای کمی داشته باشد (مثل سدیم که تنها 1 الکترون در مدار آخر خود دارد) تمایل به از دست دادن الکترون و حذف مدار آخرش دارد اما اگر تعداد الکترونهای مدار آخر یک اتم زیاد باشد (مانند کلر که 7 الکترون در مدار آخر خود دارد) تمایل به گرفتن الکترون و تکمیل مدار آخرش دارد.
خود را بیازمایید صفحه 19 علوم تجربی نهم
١- از واکنش فلز سدیم با گاز فلوئور سدیم فلوئورید به دست میآید. با توجه به نمادهای شیمیایی 9F و 11Na به پرسشهای زیر پاسخ دهید.
الف) آرایش الکترونی این دو اتم را رسم کنید.

ب) کدام یک با از دست دادن الکترون به ذرهای با مدار ۸ الکترونی تبدیل میشود؟
اتم سدیم تبدیل به یون مثبت سدیم (+Na) میشود.
پ) کدام یک با گرفتن الکترون به ذرهای با مدار ۸ الکترونی تبدیل میشود؟
یون مثبت سدیم دارای 1 عدد بار الکتریکی مثبت و یون منفی فلوئورید نیز دارای 1 عدد بار الکتریکی منفی.
ث) آیا ترکیب یونی سدیم فلورید در مجموع خنثی است؟ به چه دلیل؟
بله، زیرا میزان بار الکتریکی مثبت و منفی آن برابر میباشد.
2- با توجه به آرایش الکترونی اتمهای فلز منیزیم و اکسیژن، ذرههای سازندهٔ منیزیم اکسید (MgO) را مشخص کنید.

جواب فکر کنید صفحه 19
به شکل زیر به دقت نگاه کنید و به پرسشها پاسخ دهید.

الف) در مجموع چند گرم واکنشدهنده مصرف شده است؟
ب) چند گرم فراورده تولید شده است؟
6/19 گرم فرآورده تولید شده
پ) یکی از مهمترین قوانین طبیعی، قانون پایستگی جرم است. این قانون را در یک جمله بیان کنید.
ماده تغییر میکند ولی مقدار کلی آن در جهان ثابت است یا در واکنشهای شیمیایی همواره مقدار جرم واکنشدهندهها و مقدار جرم فرآورده ها برابر میباشد.
جواب فکر کنید صفحه 22 علوم تجربی نهم
۱- چرا تخم مرغ سالم در آب مقطر فرو میرود، اما با حل کردن نمک در آن، تخم مرغ غوطهور میشود؟
زیرا ابتدا چگالی تخم مرغ از چگالی آب مقطر بیشتر است پس تخم مرغ سالم به زیر آب رفته غوطهور میشود پس از حل شدن نمک در آب، چگالی محلول از چگالی تخم مرغ سالم بیشتر شده پس تخم مرغ سبک به بالا آمده شناور میشود.
۲- آب برخی دریاچهها مانند دریاچهٔ ارومیه بسیار شور است. به طوری که در این دریاچهها به راحتی میتوان شناور ماند و حتی روی آب، روزنامه خواند. چرا؟
زیرا چگالی آب شور دریاچه ها از چگالی بدن ما بیشتر است پس ما روی آب شناور میمانیم.
جواب خود را بیازمایید صفحه 22 علوم تجربی نهم
با توجه به شکل بالا به پرسشها پاسخ دهید.
الف) برای تشکیل یک مولکول آب، هر اتم هیدروژن چند الکترون به اشتراک گذاشته است؟
هر اتم هیدروژن یک الکترون به اشتراک گذاشته است.
ب) در مدار آخر اتم هیدروژن در مولکول آب چند الکترون وجود دارد؟
دو الکترون وجود دارد
پ) برای تشکیل یک مولکول آب، اتم اکسیژن چند الکترون به اشتراک گذاشته است؟
هر اتم اکسیژن دو الکترون به اشتراک گذاشته است.
ت) در مدار آخر اتم اکسیژن در مولکول آب چند الکترون وجود دارد؟
8 الکترون وجود دارد.
جواب خود را بیازمایید صفحه 22 علوم تجربی نهم
مولکول متان، (CH4) ، از ۴ اتم هیدروژن و یک اتم کربن تشکیل شده است. با توجه به فرمول متان:
الف) آرایش الکترونی مدار آخر اتمهای 1H و 6C را رسم کنید.
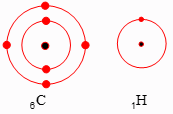
ب) نحوهٔ تشکیل مولکول متان را با رسم ساختارهای اتمی نشان دهید.
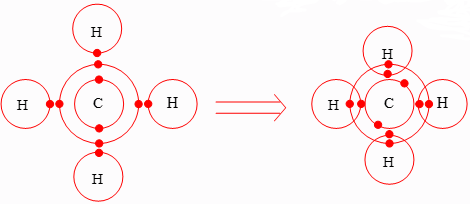
پ) هر اتم کربن چند پیوند اشتراکی میدهد؟
4 پیوند کووالانسی ایجاد میکند.
ت) هر اتم هیدروژن چند پیوند اشتراکی میدهد؟
1 پیوند کووالانسی ایجاد میکند.
جواب فعالیت صفحه 24 علوم تجربی نهم
با استفاده از مدلهای مولکولی و با فرض داشتن دو اتم کربن و تعداد کافی از اتمهای هیدروژن:
۱- سه ترکیب مولکولی ۲ کربنه بسازید.
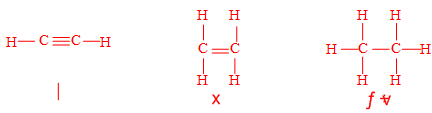
۲- مشخص کنید در ترکیبهایی که ساختهاید، هریک از اتم هایکربن چند پیوند دادهاند؟
هر اتم کربن 4 پیوند کووالانسی دارد.
۳- فرمول مولکولی هر سه ترکیب را بنویسید.
الف) C2H6 ب) C2H4 ج) C2H2


